Американский регулятор сообщил о случаях плоскоклеточного рака и лимфом после установки грудных имплантатов. Ранее FDA заявляло о возможном риске развития другого типа лимфомы при установке устройства.
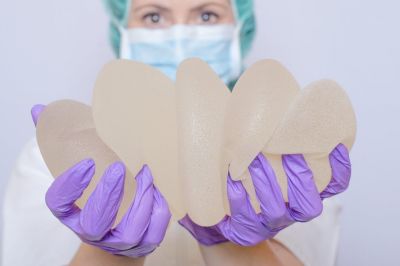
Управление по контролю за качеством пищевых продуктов и лекарственных препаратов США (FDA) сообщило о новых проблемах безопасности при установке грудных имплантатов. Регулятор сообщает об известных случаях развития плоскоклеточного рака и различных видов лимфом в капсуле или рубцовой ткани вокруг имплантатов.
Регулятору известно о 10 случаях плоскоклеточного рака и 12 лимфом, полученных из отчетов безопасности, поступивших в агентство. При анализе литературных источников в рамках текущего мониторинга выявлено около 20 случаев рака и 30 случаев различных лимфом при установке имплантатов. Новообразования выявляли в капсуле и рубцовой ткани вокруг имплантируемого устройства.
FDA оценивает риск новообразований как низкий. Но в некоторых случаях новообразования были выявлены спустя годы после установки имплантатов. Первыми признаками были отек, боль, уплотнения и изменения кожи.
Это новая проблема безопасности, уточняет FDA. В 2011 году была выявлена связь между установкой имплантируемых устройств груди и развитием анапластической крупноклеточной лимфомы.
Пока недостаточно информации, чтобы сказать, что грудные имплантаты вызывают развитие новообразований, или некоторые виды имплантируемых устройств представляют более высокий риск, уточняет FDA. Регулятор сообщает о привлечении ведущих экспертов и тщательном мониторинге различных источников данных, включая научную литературу, отчеты о нежелательных явлениях, и запрашивает информацию у производителей.
FDA заявляет о скором завершении обзора данных. Также агентство проводит консультации с Американским обществом пластических хирургов и ищет способы получения более подробной информации о пациентах с новообразованиями в капсуле при установке грудного имплантата.